Resumo
No passado, alguns pesquisadores que estudavam os efeitos do campo magnético muitas vezes os relacionavam com a ação de sensitivos sobre diversos sistemas. No entanto, nas últimas décadas percebeuse que as alterações observadas nesses sistemas deviam-se basicamente à presença de água nos mesmos. Dentre vários processos que podem alterar o comportamento da água líquida estão a ação de campos magnéticos e o processo de diluição sucessiva em soluções aquosas. Existem várias evidências de que a água tratada em campos magnéticos possui propriedades diferentes da água não tratada. Esse fato se deve ao enfraquecimento ou à quebra das ligações de hidrogênio entre as moléculas de água. No processo de dinamização observa-se que soluções diluídas apresentam absorção de luz UV numa faixa de concentração em que o soluto não é mais detectado pelo espectrômetro, o que indica a absorção de luz por possíveis arranjos do solvente a partir das dinamizações.
Palavras-chave
Campo magnético, clusters, soluções diluídas.
Abstract
In earlier times, some researchers who studied magnetic field effects related them to a psychic power influencing different systems. However, over the last decades it was realized that the alterations observed on these systems are due to the presence of water. Among the different processes that can alter the behavior of liquid water there are the action of magnetic fields and the successive dilution process of aqueous solutions. There are many evidences that the properties of magnetically treated water are different from the ones of untreated water. This fact is usually attributed to the weakness or breaking of intermolecular interactions (hydrogen-bond). It is observed that diluted solutions, prepared by dinamization process, absorbe UV light in a concentration range where the solute is no longer detected by spectrometry, which indicates a probable absorption by rearranged solvent after dinamization process.
Key-words
Magnetic field, clusters, diluted solutions.
Introdução
O termo magnetismo é utilizado desde a Antigüidade, em referência ao magnetismo animal, advindo do poder de cura de algumas pessoas específicas (“sensitivos”), assim como ao magnetismo mineral, advindo das propriedades magnéticas dos ímãs. Essa dualidade na utilização do termo deve-se a que os resultados de experimentos realizados através do magnetismo nas pessoas eram muito semelhantes àqueles provenientes da utilização de ímãs.1
Na década de 1960 Bernard Grad, da Universidade McGill de Montreal, realizou uma série de experimentos utilizando sensitivos (magnetismo animal) para verificar possíveis efeitos em ratos e plantas.3 Grad observou diferenças significativas entre os grupos tratados e os grupos controle. Os ratos tratados através do suposto magnetismo de seres vivos apresentaram um aumento na velocidade de cicatrização de feridas. Sementes irrigadas com solução tratada de NaCl apresentavam uma maior porcentagem de germinação e davam origem a plantas mais altas do que as do grupo controle (a solução 1% de cloreto de sódio inibe o crescimento vegetal). Posteriormente, Grad submeteu amostras de água ao mesmo tratamento aplicado aos ratos e às plantas e fez medidas de absorção na região do infravermelho, onde descobriu que o ângulo de ligação da molécula de água havia sofrido uma alteração sutil porém detectável, quando comparada ao controle, além de uma ligeira redução nas medidas de tensão superficial.
Na década de 1970, Robert Miller confirmou experimentalmente a descoberta de Grad a respeito das diferenças nas áreas biológica e físico-química entre propriedades da água tratada através de seres vivos (sensitivos) e a água controle.3 Miller foi um passo além quando incluiu em seus experimentos um grupo cuja água era tratada através de campos magnéticos (ímãs). Verificou as semelhanças entre as propriedades da água tratada através dos sensitivos e através do campo magnético, sendo que, em alguns casos, a água tratada com ímãs proporcionava efeitos ainda superiores àqueles obtidos pela ação dos sensitivos.
Na mesma época, Justa Smith realizou experimentos com enzimas e verificou que tanto a ação de sensitivos quanto a ação do campo magnético tinham a capacidade de aumentar as taxas de reação das enzimas.3
Como explicar essas observações? Uma possibilidade seria supor que a ação do campo magnético, assim como a ação de sensitivos, sobre um determinado sistema poderia alterar as propriedades da água presente no mesmo. Se propusermos que isso ocorre através da água, será necessário admitir que a água pode mudar suas propriedades sem a adição de solutos; e isso implica em alteração de estrutura, se quisermos manter o pensamento químico que correlaciona estrutura e propriedades para uma substância. Seria a alteração de estrutura da água a explicação para esses fenômenos e também a base para explicar a ação da homeopatia na qual, em geral, a concentração do soluto é desprezível?1
Na década de 1980, Jacques Benveniste, da Universidade de Paris, Clamart, França, e colaboradores, publicaram um artigo de grande impacto na revista Nature. O trabalho apresentava os resultados de reações de basófilos humanos com soluções anti-Ig E (anticorpos de imunoglobulina E) preparadas em sucessivas diluições (1:100 em volume) até atingir uma concentração nominal final de 2,2 x 10-126 mol L-1.4 Nessa faixa de concentração não existem mais moléculas do soluto presentes na solução e, no entanto, foram detectados picos de degranulação dos basófilos. As diluições haviam sido seguidas de posterior agitação vigorosa; a hipótese que explicaria a transmissão das informações biológicas poderia estar relacionada à organização molecular da água (solvente).1
Como as alterações observadas em sistemas que utilizam campo magnético deviam-se basicamente à presença de água nos mesmos, vários estudos que visam compreender e sistematizar a ação dos campos magnéticos iniciam-se através do estudo da estrutura da água. No entanto, ainda hoje não há um consenso a respeito dos modelos que descrevem a estrutura da água líquida e possíveis alterações de comportamento desses sistemas.1
A água
Apesar de apresentar uma estrutura simples e bem conhecida no meio científico, a água é uma substância com características muito específicas e possui um comportamento físico-químico bem distinto de substâncias com estruturas químicas semelhantes.
Considerada um solvente universal, a água constitui 80% da superfície da Terra e 70% em massa do corpo humano. A água possui valores elevados de calor específico e calor de vaporização. Essas características devem-se às fortes interações intermoleculares (ligações de hidrogênio entre as moléculas). Além disso, a água apresenta um valor de densidade máxima à 4ºC, o que permite a vida em corpos aquáticos com superfícies congeladas. Ao se congelar, a água expande-se, o que por um lado promove danos aos tecidos celulares e, por outro, gera a produção de solos férteis após o descongelamento do mesmo. São muitas as características incomuns dessa substância e a compreensão de sua estrutura não é nada trivial, principalmente na fase líquida. Para tentar elucidar essa questão citaremos dois modelos principais existentes na literatura que abordam a estrutura da água líquida.
1. Modelo Contínuo, proposto por Pople,5,6 que assume a existência de uma rede flexível formada por ligações de hidrogênio entre as moléculas de água, podendo sofrer distorções locais quando perturbada.
2. Modelo de Misturas, proposto por Némethy e Scheraga,7 que pressupõe que a cada momento uma amostra de água é composta por uma mistura de clusters de tamanhos diferentes, formados por ligações de hidrogênio, e de moléculas livres de água que não estão conectadas por ligações de hidrogênio. Esses clusters consistem em aglomerados de moléculas de água formando estruturas fechadas – (H2O)n. Anteriormente, em 1957, Frank e Wen8 descreveram um modelo no qual microcristais de gelo coexistem com a água líquida, mesmo acima da temperatura de fusão. As idéias são semelhantes, com a diferença de que os clustersde Némethy e Scheraga consistem de aglomerados menores, de cerca de 11 moléculas.
Segundo alguns trabalhos referidos na literatura,9,10 quando a água é exposta a campos magnéticos ocorre um enfraquecimento ou quebra das ligações de hidrogênio intermoleculares e, conseqüentemente, se adotarmos o modelo de misturas, torna-se possível um novo arranjo de clusters com tamanhos menores que os originais. Em princípio, podemos imaginar que clusters de tamanhos menores terão maior facilidade de permear algumas barreiras e poderão apresentar comportamentos diferentes daqueles com tamanhos maiores. Ou seja, se adotarmos o modelo de clusters para a água líquida, não poderemos mais generalizar o comportamento e propriedades da água como sendo constituída simplesmente de moléculas H2O mas, devemos levar em consideração a média da sua distribuição de tamanho de clusters (H2O)n.
Para evidenciarmos indiretamente a possível quebra dos clusters em uma amostra apresentamos alguns resultados experimentais que mostram novos comportamentos da água tanto após a exposição ao campo magnético como através de processos de dinamização (diluição sucessiva seguida de agitação vigorosa ou sucussão).
Resultados experimentais
1. Alterações do comportamento da água em diversos sistemas após a exposição ao campo magnético:
Faigle e Barboza,11,12 estudaram a influência de diferentes intensidades de campos magnéticos sobre a formação e nucleação de carbonato de cálcio (CaCO3). Os autores observaram, entre outras coisas, que os cristais de CaCO3 dos grupos controle eram em média maiores e em menor quantidade que os dos grupos tratados, como mostra a Figura 1. Nesse caso, os íons Ca+2 e CO32- e suas respectivas duplas camadas elétricas sofrem o efeito do campo magnético e são deslocados de suas “trajetórias”, de modo que as partículas com cargas positivas e negativas tendem a ir para direções opostas, dificultando assim a nucleação e crescimento dos cristais11 (efeito devido à Força de Lorentz: força exercida sobre uma partícula carregada em movimento10).
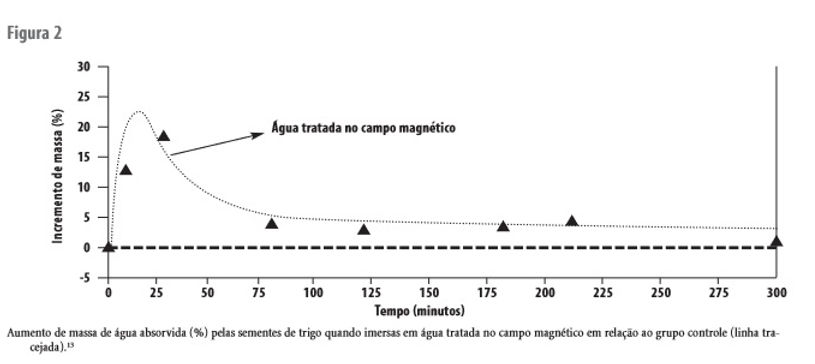
O tratamento prévio da água em campo magnético para posterior utilização no intumescimento e germinação de sementes de trigo foi estudado por Faigle e Porto.13,14 Os experimentos visaram verificar a diferença na permeação da água tratada no campo através das sementes em relação ao grupo controle e posterior germinação. As sementes de trigo utilizadas (Triticum durum, BRS-12199) foram obtidas da EMBRAPA/TRIGO – RS – Brasil, com certificação de 95% de taxa de germinação e livre de agentes patogênicos. Os testes de intumescimento foram feitos em lotes de 6.00 g de sementes de trigo, o equivalente a aproximadamente 150 unidades. Os valores de intumescimento das sementes foram obtidos através do cálculo de incremento de massa das sementes medidos em intervalos regulares de 30 minutos, durante um período total de 5 horas. Os valores de massa foram obtidos após uma secagem leve das sementes em papel de filtro. Cada experimento foi realizado em triplicata, totalizando 450 sementes utilizadas para cada amostra de água (controle e água tratada). Todas as normas de germinação foram seguidas de acordo com critérios adotados pelo Ministério da Agricultura.15
Observa-se na Figura 2 um aumento na velocidade de permeação da água tratada nas sementes em relação ao controle. O grupo tratado absorve rapidamente a água nos primeiros 25 minutos do experimento, representado pelo pico de massa de água em relação ao controle (linha tracejada). Em seguida, essa diferença entre a absorção de água pelos grupos tratado e controle diminui até manter-se pequena e constante após os 150 minutos do início do experimento. A Figura 3 mostra fotos no 4º dia de germinação das plântulas de trigo evidenciando que o grupo tratado apresenta plântulas com uma altura média superior ao grupo controle.13
Assim como a água tratada no campo magnético apresentou um aumento na velocidade de permeação de água através das sementes de trigo com relação ao grupo controle, podemos imaginar que o mesmo mecanismo possa ser observado na cinética de permeação de água através da pele humana.1,13 Essa experiência traz um desafio adicional, uma vez que a água é aplicada uma única vez sobre a pele humana e tende a evaporar, ao contrário do que ocorre com a semente que fica imersa na água por algumas horas. Existe, portanto, uma competição entre a cinética de permeação da água tratada através da pele e o processo de evaporação da água.
Para que ocorra uma hidratação efetiva da pele é necessário que uma certa quantidade de água consiga penetrar o estrato córneo antes de evaporar. Por que o simples ato de molhar a pele não produz hidratação? Provavelmente, porque a água evapora antes que consiga permear a pele. Isso pode ser evidenciado mantendose uma compressa úmida numa região da pele por longo tempo, o que produz hidratação local mensurável. Uma das possíveis interpretações para esse fato é admitir que apenas os clusters menores presentes naturalmente em pequena quantidade na água usual conseguem vencer os efeitos criados pela função de barreira da pele. Nesse caso, qualquer processo que consiga quebrar os clusters de água produzindo uma amostra estável e com clusters menores deverá penetrar a pele humana mais rapidamente. A Figura 4 mostra o incremento de hidratação da pele após a aplicação das seguintes amostras: água tratada em campo magnético, hidratante (constituído por água tratada no campo magnético com posterior adição de 0,5 ppm de MgCl2) e o hidratante diluído a 3% em água desionizada.1,13
Algumas medidas físico-químicas da água tratada no campo magnético também evidenciam alterações de propriedades em relação ao grupo controle. De maneira geral, a água exposta ao campo possui valores mais elevados de condutividade elétrica do que a água não tratada. Como exemplo, podemos citar valores médios de 8 medidas de condutividade elétrica (k) da água exposta ao campo magnético e do controle obtidos a temperaturas entre 22°C e 24°C, preparadas em 8 experimentos distintos: controle, k= 1,50 ± 0,18 µS cm-1 e água tratada, k = 2,60 ± 0,30 µS cm-1.
Zhou9 afirma que o campo magnético é capaz de quebrar ligações de hidrogênio e, portanto, favorecer a formação de novos aglomerados de água. Se esses aglomerados forem em média menores do que os aglomerados originais essa nova distribuição de tamanho dos aglomerados de água possivelmente interfira menos na trajetória dos íons transportadores de carga, fazendo com que a condutividade elétrica aumente.
2. Absorção de luz na região do ultravioleta (UV) por soluções de MgCl2 obtidas através do processo de dinamização:
Neste estudo utilizou-se a técnica de dinamização em escala centesimal progressiva (método dos frascos separados).16 Partiu-se de uma solução aquosa de cloreto de magnésio 1% que sofreu 250 sucussões manuais, denominada de dinamização centesimal 1 ou dinamização 1CH. A partir dessa solução dinamizada 1CH preparou-se as dinamizações subseqüentes seguindo-se sempre o mesmo critério de diluição a 1% da solução anterior em 99% de água destilada, seguida de 250 sucussões manuais. Preparou-se as dinamizações em frascos de vidro idênticos (marca pyrex) com tampas esmerilhadas, utilizados apenas para este experimento. Os vidros foram deixados em repouso em ambiente termostatizado a 20oC. Não foi utilizado etanol nas preparações das dinamizações para que o solvente utilizado tivesse o comportamento de uma substância pura, servindo assim como padrão e referência para os outros espectros e proporcionando análises mais confiáveis dos resultados obtidos. Nesse experimento os cuidados de limpeza e manuseio das soluções é extremamente rigoroso e mais detalhes encontram-se nas referências citadas.13,16
É interessante notar que, ao se fazer uma análise das curvas de absorção das soluções de MgCl2, partindo-se da 1CH até a 3CH, ocorre uma diminuição progressiva da absorção da radiação UV devido à respectiva diminuição de concentração do soluto, até atingir o valor de absorção diferencial zero, o que significa que a absorção das soluções dinamizadas são equivalentes às das soluções controle (essas curvas não estão apresentadas nesse trabalho mas podem ser encontradas na referências citadas13,16). Normalmente, o experimento é interrompido neste ponto, pois o equipamento não é mais sensível à quantidade de soluto presente na amostra. Se, porventura, continuarmos a realizar medidas de absorção de luz UV de soluções mais diluídas observa-se, surpreendentemente, um novo aumento de absorção de luz UV. A Figura 5 apresenta valores correspondentes à área sob a curva de absorção de luz UV para as soluções de MgCl2 dinamizadas com concentrações nominais entre ~10-5 mol L-1 à 10-19 mol L-1 (que correspondem às soluções 3CH à 10CH). Os pontos em branco da curva representam soluções dinamizadas fora da escala centesimal.13
Por que motivo as soluções mais diluídas de MgCl2 apresentam uma absorção de luz UV? Cálculos teóricos para a energia de clusters de água no estado fundamental e no estado excitado foram apresentados independentemente na literatura por Zvereva17 e Harvey18. Segundo os dados teóricos, clusters menores absorvem em regiões de comprimento de onda maiores (monômeros, dímeros e trímeros absorvem na faixa de 200 nm a 300 nm18). Se houve uma quebra de tamanhos de clusters, seja através da dinamização ou por tratamento magnético, deve-se observar um aumento da absorção de luz UV nessa região devido ao suposto aumento de número de espécies absorventes em tais comprimentos de onda.
Conclusões
A partir de estudos teóricos e experimentais pode-se concluir que a ação de campos magnéticos e o processo de dinamização em soluções aquosas pode induzir novas propriedades à água que independem da presença do soluto. Provavelmente esse comportamento se deve a reestruturações locais da água que alteram a distribuição de tamanho de clusters. A água com uma nova distribuição de tamanho de clusters adquire novas propriedades, com um grande potencial para novas aplicações.
Referências:
1. Faigle JFG, Porto MEG. O campo magnético e a água. Revista Brasileira de Ensino de Química. 2006; 1 (2): 9-24.
2. Medeiros e Albuquerque JJ. Hipnotismo. 5ª ed. Rio de Janeiro: Conquista; 1954.
3. Gerber R. Medicina vibracional. São Paulo: Editora Cultrix Ltda; 1997.
4. Davenas E, Beauvais F, Amara J, Oberbaum M, Robinzon B, Miadonnai A, et al. Human basophil degranulation triggered by very dilute antiserum against IgE. Nature. 1988; 333: 816-818.
5. Pople JA. The molecular orbital theory of chemical valency. V. The structure of water and similar molecules. Proc. R. Soc. London, A202. 1950; 323-336.
6. Pople JA. Molecular association in liquids. II. A theory of the structure of water. Proc. R. Soc. London, A205. 1951; 163-178.
7. Némethy G, Scherage HA. Structure of water and hydrophobic bonding in proteins. I. A model for the thermodynamic properties of liquid water. J.Chem. Phys. 1962; 36: 3382-3400.
8. Frank HS, Wen WY. III. Ion-Solvent Interaction. Structural aspects of ion-solvent interaction in aqueous solutions: a suggested picture of water structure. Discuss. Faraday Soc. 1957; 24: 133-140.
9. Zhou KX, Lu GW, Zhou QC, Song JH, Jiang ST, Xia HR. Monte Carlo simulation of liquid water in a magnetic field. J. Appl. Phys. 2000; 88 (4): 1802-1805.
10.Kochmarshy V. Magnetic treatment of water: possible mechanisms and conditions for applications. Mag. Electrical Sep. 1996; 7: 77-107.
11.Barboza MA. Ação de campos magnéticos em alguns sistemas químicos e biológicos. 2002. Tese (Mestrado). Instituto de Química, Universidade Estadual de Campinas - Unicamp, Campinas.
12.Barboza MA, Faigle JFG. Influência do campo magnético na cristalização de carbonato de cálcio. 24ª Reunião da Sociedade Brasileira de Química - SBQ, Poços de Caldas, M.G., 28-31 de maio de 2001.
13.Porto MEG. Alterações de propriedades da água por processos físicos e químicos. 2004. Tese (Doutorado). Instituto de Química, Universidade Estadual de Campinas - Unicamp, Campinas.
14.Faigle JFG, Porto MEG. Água estruturada: mudanças em propriedades físico-químicas e biológicas. XVIII Encontro Regional da Sociedade Brasileira de Química. Lavras, M.G., 3-5 de novembro de 2004.
15.Ministério da Agricultura e Reforma Agrária. Regras para Análise de Sementes. Brasília, DF, 1992.
16.Faigle JFG, Porto MEG, Barboza MA. Evidências de estruturação da água em soluções de diluídas de cloreto de magnésio. Revista de Homeopatia da AMHB. 2002; 4: 6-11.
17. Zvereva NA. Intermolecular hidrogen bond and its spectroscopic manifestation in formation of small water complexes. Russ. Phys. J. 1999; 42 (9): 860-864.
18.Harvey JN, Jung JO, Gerber RB. Ultraviolet spectroscopy of water clusters: excited electronic states and absorption line shapes of (H2O)n, n= 2-6. J. Chem. Phys. 1998; 109: 8747-8750.